EMMY
Epidémiologie de la prise en charge thérapeutique du myélome multiple en France
Type d'essai : Académique / Institutionnel
Etat de l'essai : Ouvert
Situation thérapeutique : Hématologie ( De Novo , Rechute/Réfractaire )
Etablissement(s) participant(s)
Dr Régis KAPHAN
Dr Laurence LEGROS
Dr Abdelaziz CHAIB
Dr Jean GUTNECHT
Dr Borhane SLAMA
Détails de l'essai
Objectif principal
Décrire l’ensemble des prises en charge thérapeutiques, en termes de protocoles thérapeutiques utilisés pour chaque ligne de traitement, chez des patients atteints de MM et traités à l’hôpital, du diagnostic initial jusqu’à la fin de leur dernière année de collecte.
Objectif(s) secondaire(s)
Décrire les caractéristiques de patients (sociodémographiques, antécédents, comorbidités, tableau clinique, etc) traités pour un MM selon les prises en charges proposées.
PFS (survie sans progression).
TNT ( temps jusqu’au traitement suivant).
OS (survie globale).
Taux de réponse.
Arrêts définitis de traitement et les motifs d’arrêt.
Décrire à partir des données de remboursement issues du SNDS, le recours au système de soins des patients pour la prise en charge du MM.
Evoluer au cours des années d’étude les évolutions des pratiques.
Résumé / schéma de l'étude
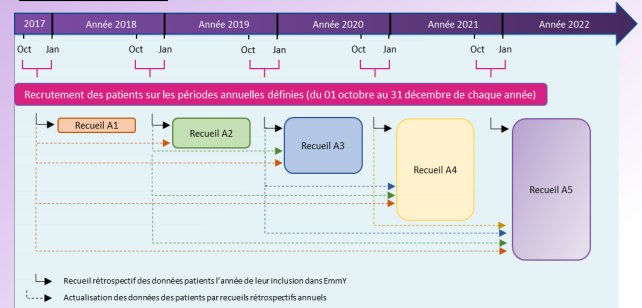
Critère(s) d'inclusion
- Patient âgé de 18 ans ou plus.
- Patient présentant un myélome multiple symptomatique ayant nécessité l’initiation (au moins une dose) d’un traitement systémique pour le myélome multiple, toutes lignes confondues, sur la période annuelle d’observation (1er octobre-31 décembre).
- Myélome multiple mesurable défini par au moins un de ces critères :
- Immunoglobuline monoclonale ≥ 5 g/l.
- Protéine monovlonale urinaire ≥ 200 mg/24h.
- Présence dans le sérum d’une chaîne légère ≥ 100 mg/l.
- Patient ayant été informé des conditions de réalisation de l’étude.
Critère(s) de non-inclusion
- Patient traité pour un MM non excrétant.
- Patient traité pour un MM asymptomatique.
- Patient traité pour un plasmocytome solitaire ou une leucémie à plasmocytes.
- Patient s’opposant à l’informatisation de ses données.
- Patient pour lequel le dossier médical n’est pas accessible.
- Patient participant à un essai clinique à l’initiation de la ligne de traitement justifiant l’inclusion dans cette étude.
- Patient ayant déjà été inclus par un autre centre.
Calendrier prévisionnel
Lancement de l’étude : Janvier 2018
Fin estimée des inclusions : Janvier 2024 (poursuite des inclusions)
Nombre de patients à inclure : 800
Promoteur de l'étude
Intergroupe Francophone du Myélome (IFM)
