OliGRAIL
Première ligne thérapeutique standard incluant l’immunothérapie associée aux traitements locauxablatifs pour les patients atteints de cancer bronchique non à petites cellules oligométastatique : une étude de phase III randomisée, ouverte, multicentrique
Type d'essai : Académique / Institutionnel
Etat de l'essai : Ouvert
Situation thérapeutique : Tumeur solide ( Métastatique / Rechute )
Etablissement(s) participant(s)
Dr Nicolas POUREL
Détails de l'essai
Objectif principal
Démontrer le bénéfice en termes de survie de l’ajout d’un traitement local ablatif (RLT) sur un maximum de 5 lésions secondaires chez les patients atteints d’un CBNPC recevant une immunothérapie basée sur les standards de soins.
Objectif(s) secondaire(s)
Comparer la survie sans progression (SSP), la survie sans progression immunitaire (iSSP), la survie spécifique liée au cancer, les types de rechute entre les deux bras.
Comparer la fréquence et la gravité des événements indésirables entre les deux bras.
Comparer les résultats rapportés par les patients (PRO) / la qualité de vie (QoL).
Evaluer l’élimination de l’ADN tumoral circulant.
Evaluer le rapport coût-utilité (coût par QALY) du traitement standard basé sur l’immunothérapie + RLT par rapport au traitement standard seul (évaluation économique).
Explorer l’effet des RLT (chirurgie mini-invasive vs radiothérapie stéréotaxique (SBRT) vs radiologie interventionnelle) sur la survie globale (SG) et le contrôle local.
Résumé / schéma de l'étude
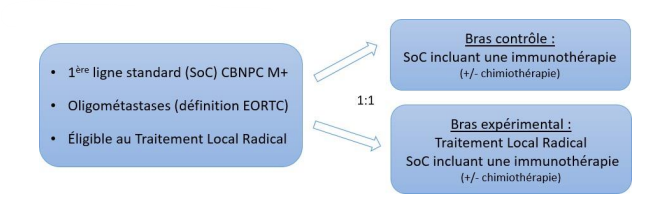
Critère(s) d'inclusion
- Patient âgé de 18 ans ou plus.
- CBNPC oligométastatique synchrone avancé de stade IV, prouvé histologiquement.
- CBNPC éligibles à un traitement standard à base d’immunothérapie de première intention selon l’autorisation de mise sur le marché européen et avec un statut PDL1 disponible.
- Métastases éligibles au RLT selon le la réunion de concertation pluridisciplinaire (RCP) locale :
- ≤ 5 cm chacune au scanner, hors tumeur primitive.
- Maximum de 5 métastases dans 3 organes (critères EORTC), selon IRM cérébrale et TEP-FDG.
- Les lésions symptomatiques nécessitant une radiothérapie palliative urgente sont autorisées avant la randomisation. Ces lésions traitées doivent être comptabilisées dans le nombre total de métastases au moment de l’inclusion.
- Le traitement de métastases cérébrales (MC) symptomatique (chirurgie et/ou SBRT) est autorisée et la MC doit être comptabilisée dans le nombre total de métastases lors de l’inclusion. Le patient serait ensuite randomisé pour recevoir le traitement de sa maladie extracrânienne.
- Fonction d’organe acceptable pour un RLT.
- Statut de performance ECOG (PS) 0-1.
- Lésions mesurables par imagerie standard selon RECIST V1.1.
- Les femmes en âge de procréer doivent accepter d’utiliser une contraception adéquate (implant, anneau vaginal, pilule contraceptive, patch contraceptif, dispositif intra-utérin (DIU), etc.) pendant toute la durée de la participation à l’étude et jusqu’à 6 mois après la fin du traitement/thérapie, de plus, les partenaires masculins doivent utiliser un préservatif pendant cette même période. Les patients masculins doivent accepter d’utiliser un préservatif pendant toute la durée de leur participation à l’étude et jusqu’à 6 mois après la fin du traitement/de la thérapie.
- Le patient doit comprendre, signer et dater le formulaire de consentement éclairé rédigé en français avant toute procédure spécifique au protocole effectuée.
Critère(s) de non-inclusion
- CBNPC non épidermoïde avec mutations tumorales ciblables et thérapie ciblée de première intention approuvée (telle que EGFR, ALK et ROS1).
- Métastases non éligibles au RLT : par exemple, métastases du tronc cérébral ou métastases séreuses diffuses (méningées, péricardiques, pleurales, péritonéales, mésentériques) ou qui envahissent le tractus gastro-intestinal, métastases cérébrales uniquement, sans métastases extra-cérébrales.
- Comorbidité sévère non contrôlée, maladie pulmonaire interstitielle symptomatique ou infection active.
- Traitement antérieur par co-stimulation des lymphocytes T ou agents ciblés sur les points de contrôle immunitaire dans un délai d’un an.
- Tumeur maligne concomitante non contrôlée (<1 an), sauf carcinome basocellulaire ou épidermoïde de la peau correctement traitée, ou carcinome in situ de tout organe ou mélanome in situ de la peau.
- Les lésions symptomatiques nécessitant une radiothérapie palliative urgente sont autorisées avant la randomisation. Ces lésions traitées doivent être comptabilisées dans le nombre total de métastases au moment de l’inclusion.
- Personnes privées de liberté par décision judiciaire ou administrative.
- Personnes soumises à une mesure de protection juridique (tutelle, curatelle, sauvegarde de justice).
- Personnes non affiliées à un régime de sécurité sociale ou équivalent.
Calendrier prévisionnel
Lancement de l’étude : Septembre 2025
Fin estimée des inclusions : Février 2030
Nombre de patients à inclure : 124
Coordonnateur de l'étude
Dr Antonin LEVY – Gustave Roussy – CLCC Villejuif
Promoteur de l'étude
Gustave Roussy – CLCC Villejuif
