Prodige 112 -NACRE 2
Etude de phase III, randomisée, évaluant deux stratégies de traitement pour le cancer rectal localement avancé, chez des patients de 75 ans et plus
Type d'essai : Académique / Institutionnel
Etat de l'essai : Ouvert
Situation thérapeutique : Tumeur solide ( Adjuvant )
Etablissement(s) participant(s)
Dr Ludovic EVESQUE
Détails de l'essai
Objectif principal
Comparer l’efficacité d’une radiothérapie 5*5 suivie de 6 cycles de chimiothérapie FOLFOX versus radiothérapie 5*5 sans chimiothérapie, en termes de taux de préservation d’organe, chez des patients âgés avec un cancer rectal localement avancé (cT3-T4).
Objectif(s) secondaire(s)
Taux de réponse complète clinique (cCR) à 21 semaines.
Survie globale (SG) à 24 mois.
Taux d’échec locorégional à 24 mois.
Survie sans maladie (SSM) à 24mois.
Taux de réapparition locale à 24 mois.
Survie sans métastase à 24 mois.
Taux de résection R0.
Taux de complications postopératoires de la chirurgie initiale à 3 mois.
Taux de complications postopératoires de la chirurgie de sauvetage après une NOM initiale à 3 mois.
Profil de sécurité.
Dysfonction intestinale à l’inclusion, 3 mois post-radiothérapie, 12 mois et 24 mois après inclusion.
Qualité de vie à l’inclusion, 3 mois post-radiothérapie, 12 mois et 24 mois après inclusion.
Evaluation gériatrique à l’inclusion, 3 mois post-radiothérapie, 12 mois et 24 mois après inclusion.
Résumé / schéma de l'étude
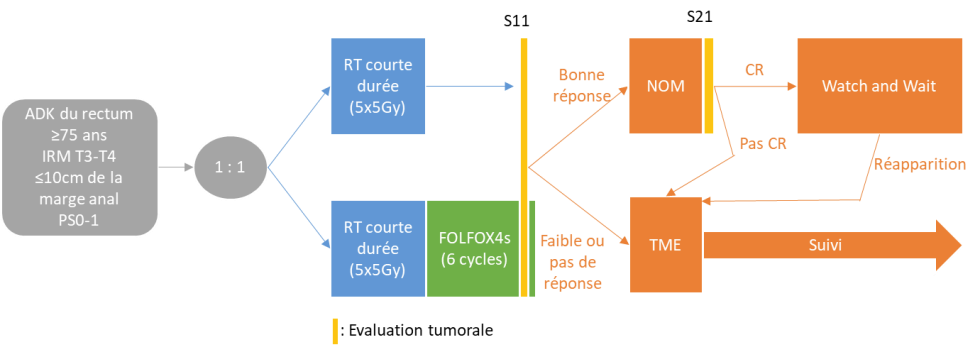
Critère(s) d'inclusion
- Diagnostic d’adénocarcinome du rectum, confirmé histologiquement.
- Age ≥ 75 ans.
- Score de performance ECOG 0-1.
- Tumeur de stade cT3a-b avec diamètre maximal > 5 cm, ou T3c-d ou cT4 sur l’IRM pelvienne avant traitement.
- Condition générale considérée comme adaptée à une chirurgie pelvienne radicale et à un traitement systémique par FOLFOX.
- Extrémité distale de la tumeur située à ≤10 cm de la marge anale, selon la mesure effectuée par rectoscopie rigide ou à l’IRM pelvienne.
- Approbation d’un oncogériatre.
- Fonction biologique acceptable, définie par :
a. Neutrophiles ≥ 1500/mm3
b. Plaquettes ≥ 100 000/mm3
c. Hémoglobine ≥ 10g/dL
d. Bilirubine ≤ 1,5 x LSN
e. Phosphatase alcaline ≤ 1,5 x LSN
f. Clairance de la Créatinine >50mL/mn (MDRD)
g. Taux d’aspartate aminotransférase (AST) et d’alanine aminotransférase (ALT) ≤ 2,5 × LSN - Les hommes doivent accepter d’utiliser des méthodes contraceptives adéquates pendant pendant le traitement par oxaliplatine et au moins jusqu’à 12 mois après la fin de ce traitement.
- Les patients doivent être affiliés à un système de sécurité sociale (ou équivalent).
- Le patient doit avoir signé un consentement éclairé écrit avant toute procédure spécifique à l’essai. Lorsque le patient est physiquement incapable de donner son consentement écrit, une personne de confiance de son choix, indépendante de l’investigateur ou du promoteur, peut confirmer par écrit le consentement du patient.
- Les patients doivent être disposés et capables de se conformer au protocole pendant toute la durée de l’étude, y compris les visites prévues, le plan de traitement, les tests de laboratoire et les autres procédures de l’étude.
Critère(s) de non-inclusion
- Maladie métastatique.
- Antécédent de cancer dans les 3 ans précédant le diagnostic de cancer rectal (à l’exception des cancer in situ et des carcinomes cutanés basocellulaires.
- Cancer non résécable, y compris extension à la prostate ou extension aux muscles périnéaux.
- Antécédent d’irradiation pelvienne.
- Contre-indication à la chimiothérapie FOLFOX 4s :
Concernant le traitement par 5-fluorouracile :
• Traitement récent (au cours des 4 dernières semaines) ou concomitant par brivudine
• Présence d’une infection potentiellement grave
• Administration d’un vaccin vivant ou vivant atténué dans les 30 jours précédant la première dose de l’intervention de l’étude
• Mauvais état nutritionnel / Maladie cardiaque active cliniquement significative ou infarctus du myocarde au cours des 6 derniers mois, compte tenu de la cardiotoxicité du fluorouracile
Concernant le traitement par oxaliplatine :
En raison de la cardiotoxicité de l’oxaliplatine (risque de prolongation du QT tel que décrit à la section 4.4 de la RCP de l’oxaliplatine) :
• Hypokaliémie inférieure à la normale
• Hypomagnésémie
• Hypocalcémie • Intervalle QT/QTc supérieur à 450 ms chez l’homme et supérieur à 470 ms chez la femme à l’ECG d’inclusion
• Neuropathie sensorielle périphérique avec atteinte fonctionnelle avant le premier traitement, conformément à la RCP de l’oxaliplatine
• Antécédent connu d’hypersensibilité au fluorouracile, à l’oxaliplatine, à l’acide folinique ou à l’un de leurs excipients, comme indiqué dans les RCP respectives - Contre-indication à la radiothérapie et/ou à la chirurgie TME.
- Contre-indication à l’IRM.
- Instabilité Microsatellitaire (MSI) et/ou déficience dMMR.
- Déficience complète ou partielle en Dihydropyrimidine deshydrogenase (DPD) (uracilémie ≥ 16 ng/mL).
- Événement thrombo-embolique artériel ou veineux comme un accident vasculaire cérébral (y compris les ischémies transitoires), une thrombose veineuse profonde ou une embolie pulmonaire, pendant les 6 mois précédant le début du traitement.
- Tout autre trouble ou maladie concomitant susceptible d’interférer avec la participation du patient ou sa sécurité pendant l’étude (par ex., trouble sévère hépatique, cardiaque, rénal, pulmonaire, métabolique ou psychiatrique).
- Traitement par un autre médicament expérimental ou anti-cancéreux dans les 30 jours avant la randomisation.
- Tout trouble psychiatrique empêchant la compréhension de l’information des sujets liés à l’étude, et d’exprimer un consentement éclairé.
- Chimiothérapie ou chirurgie antérieure du cancer rectal.
- Tout condition médicale sérieuse (selon le jugement de l’investigateur) risquant d’altérer la capacité du patient à participer à l’étude.
- Personne privée de liberté ou placée sous tutelle ou curatelle.
- Impossibilité d’effectuer le suivi médical requis pour des raisons géographiques, sociales ou psychologiques.
Calendrier prévisionnel
Lancement de l’étude : Avril 2026
Fin estimée des inclusions : Avril 2029
Nombre de patients à inclure : 160
Coordonnateur de l'étude
Dr Ludovic EVESQUE – Centre Antoine Lacassagne – CLCC Nice
Promoteur de l'étude
UNICANCER
